Periodiska Systemet -> tryck här
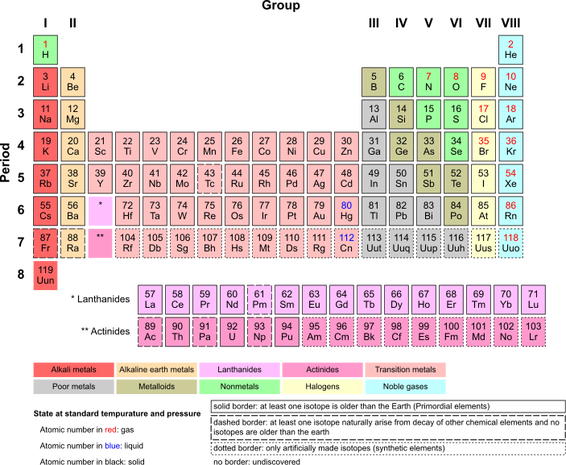
Det Periodiska systemet är sätt att lära sig gemensamma egenskaper hos atomer. Första gången kan det periodiska systemet kännas mycket komplicerat, men så är faktisk inte fallet. Det följer några enkla regler och genom att lära sig dessa regler går det att förstå otroliga mängder kemi.
I alla ruter, bredvid, står det en bokstav och en siffra. Bokstaven är förkortningen på ämnet och siffran är vilken ordning ämnet uppkommer i periodiska systemet.
Som ex. har vi första rutan där det står en etta och ett H. Ettan betyder att det är det första ämnet och därmed även det lättaste ämnet . H betyder väte (på engelska heter väte hydrogen, därav förkortningen H) och är förkortningen på ämnet.
Direkt under H står det Li och en trea, vilket står för Lithium och att det är det tredje ämnet i det periodiska systemet. Går vi vidare nedåt finner vi Na, K, Rb osv. Alla ämnen som står på detta sätt bildar det som kallas för grupp (kolumn).
Om vi går tillbaka till det första ämnet d.v.s. H (väte) och så försöker vi finna det ämnet som har nummer två finner vi att det står längst upp till höger. Detta ämne har förkortningen He (helium). He tillsammans med H (väte) bildar en det som brukar kallas för period (rad). Nedan kommer vi gå igenom vad reglerna säger om ämnen som står i en specifik rad och kolumn samt förklara vad ämnets nummer betyder.
Varje ämne har ett nummer väte (H) har siffran 1, helium (He) har siffran 2, kol (C) har siffran 6 osv. Dessa siffror betyder hur många protoner (+) och elektroner (-) som finns i ämnet. Så nu vet vi att väte (H) med siffran 1 har alltså en proton och en elektron, helium (He) med siffran 2 har två protoner och två elektroner, samt
kol (C) med siffran 6 har sex protoner och sex elektroner. Tänk efter hur många protoner och elektroner guld (Au) har?
Vidare så finns varje ämne i en specifik period och grupp. Vilken period ett ämne finns i bestämmer hur många elektronskal atomen har, medan gruppen säger hur många valenselektroner (elektronerna i det yttersta skalet) det finns i atomen.
Om vi tar och jämför litium (Li) och kol (C) så ser vi i bilden ovan att Li finns i grupp 1 och i period 2. Detta säger alltså att Li har en valenselektron men den har två elektronskal. Vad blir det med kol då?
I alla ruter, bredvid, står det en bokstav och en siffra. Bokstaven är förkortningen på ämnet och siffran är vilken ordning ämnet uppkommer i periodiska systemet.
Som ex. har vi första rutan där det står en etta och ett H. Ettan betyder att det är det första ämnet och därmed även det lättaste ämnet . H betyder väte (på engelska heter väte hydrogen, därav förkortningen H) och är förkortningen på ämnet.
Direkt under H står det Li och en trea, vilket står för Lithium och att det är det tredje ämnet i det periodiska systemet. Går vi vidare nedåt finner vi Na, K, Rb osv. Alla ämnen som står på detta sätt bildar det som kallas för grupp (kolumn).
Om vi går tillbaka till det första ämnet d.v.s. H (väte) och så försöker vi finna det ämnet som har nummer två finner vi att det står längst upp till höger. Detta ämne har förkortningen He (helium). He tillsammans med H (väte) bildar en det som brukar kallas för period (rad). Nedan kommer vi gå igenom vad reglerna säger om ämnen som står i en specifik rad och kolumn samt förklara vad ämnets nummer betyder.
Varje ämne har ett nummer väte (H) har siffran 1, helium (He) har siffran 2, kol (C) har siffran 6 osv. Dessa siffror betyder hur många protoner (+) och elektroner (-) som finns i ämnet. Så nu vet vi att väte (H) med siffran 1 har alltså en proton och en elektron, helium (He) med siffran 2 har två protoner och två elektroner, samt
kol (C) med siffran 6 har sex protoner och sex elektroner. Tänk efter hur många protoner och elektroner guld (Au) har?
Vidare så finns varje ämne i en specifik period och grupp. Vilken period ett ämne finns i bestämmer hur många elektronskal atomen har, medan gruppen säger hur många valenselektroner (elektronerna i det yttersta skalet) det finns i atomen.
Om vi tar och jämför litium (Li) och kol (C) så ser vi i bilden ovan att Li finns i grupp 1 och i period 2. Detta säger alltså att Li har en valenselektron men den har två elektronskal. Vad blir det med kol då?
